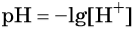Определение характера среды раствора кислот и щелочей с помощью индикаторов. Качественные реакции на ионы в растворе (хлорид-, сульфат-, карбонат-ионы, ион аммония)

Термин рН — водородный показатель — это отрицательный десятичный логарифм концентрации ионов водорода, выраженной в моль/л:
Если pH = 7 — реакция растворов нейтральная, pH > 7 — реакция растворов щелочная, pH < 7 — реакция растворов кислая.
Цвета индикаторов в зависимости от характера среды.
Лакмус в кислой среде — красный; в нейтральной — фиолетовый; в щелочной — синий.
Метиловый оранжевый в кислой среде — красный, в щелочной — жёлтый.
Фенолфталеин в кислой и нейтральной среде — бесцветный; в щелочной — малиновый.
Химия является наукой о веществах и их превращениях. Для исследования, описания и идентификации различных химических веществ применяют различные методы качественного и количественного анализа, инструментальные методы исследования.
Качественный анализ позволяет установить, какие именно ионы входят в состав данного вещества.
Таблица качественных реакций на различные катионы и анионы приведена в приложении в конце 7 урока.
Так, качественной реакцией на хлорид-ион является выделение белого осадка при взаимодействии с нитратом серебре. Сульфат-ионы определяют по образованию осадка белого цвета при взаимодействии с растворимыми солями бария. Для определения карбонат-ионов проводят с помощью кислот. При этом происходит выделение бесцветного газа, не имеющего запаха, но вызывающего помутнение известковой воды.
Качественной реакцией на ион аммония является выделение бесцветного газа с характерным запахом и вызывающего изменение цвета индикаторной бумаги в парах при взаимодействии солей аммония с растворами щелочей.