Урок 15. Воздух как смесь газов
В уроке 15 «Воздух как смесь газов» из курса «Химия для чайников» мы выясним из чего состоит воздух; узнаем о получении, собирании и хранении газов, а также об их герметичности.
Вы уже знаете, что вещества могут находиться в различных агрегатных состояниях: газообразном, жидком и твердом.
В окружающей нас природе многие вещества при обычных условиях находятся в газообразном состоянии. Прежде всего, это компоненты воздушной оболочки Земли — атмосферы. Очень много газов растворено в водах Мирового океана. Во время извержения вулканов в атмосферу также выбрасывается большое количество вулканических газов. В недрах нашей планеты хранятся огромные запасы природного газа.
Атмосфере принадлежит важнейшая роль в жизни человека, животных и растений. Ее исследованиям были посвящены труды многих ученых прошлого. С давних времен был известен лишь один вид газа — воздух. При этом он изучался в основном физиками и интереса у химиков не вызывал. Лишь во второй половине XVIII в. было установлено, что воздух представляет собой смесь газов.
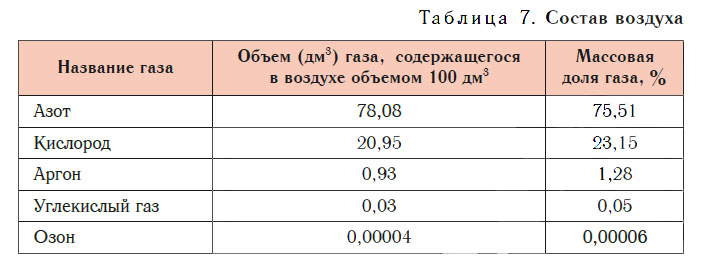
Состав воздуха
Основные компоненты воздуха — азот и кислород. При нормальных условиях в воздухе объемом 100 дм3 содержится азот объемом около 78 дм3 и кислород объемом около 21 дм3, а на долю всех остальных газов приходится около 1 дм3. В заметных количествах в воздухе присутствуют аргон, углекислый газ, озон и другие газы (табл. 7).
Для решения некоторых задач и проведения расчетов в физике, химии, технике очень удобно рассматривать воздух не как смесь газов, а как одно газообразное вещество. Экспериментальным путем можно установить, что при нормальных условиях масса воздуха объемом 22,4 дм3 равна 29 г. Поскольку такой объем при н. у. занимает любой газ химическим количеством 1 моль, то молярную массу воздуха можно условно считать равной 29 г/моль:
Все газы, молярная масса которых меньше 29 г/моль, принято называть газами легче воздуха (например, водород H2, аммиак NH3, угарный газ CO, метан CH4), а газы, у которых она больше 29 г/моль — газами тяжелее воздуха (например, кислород O2, озон O3, углекислый газ CO2).
Получение, собирание и хранение газов
Газы имеют важное значение в жизни и деятельности человека. Поэтому необходимо уметь их получать, собирать и хранить.
В химической лаборатории небольшие объемы газов можно получать различными способами. Например, газы выделяются при нагревании некоторых твердых веществ (рис. 66).
Газообразные вещества могут образовываться при действии некоторых жидких веществ на твердые. Так, при действии уксуса на мрамор или мел выделяется углекислый газ (рис. 67).
В промышленности используют значительно большие, чем в химических лабораториях, количества различных газов. Большие объемы кислорода и азота получают из воздуха. Позднее вы узнаете, как это делается.
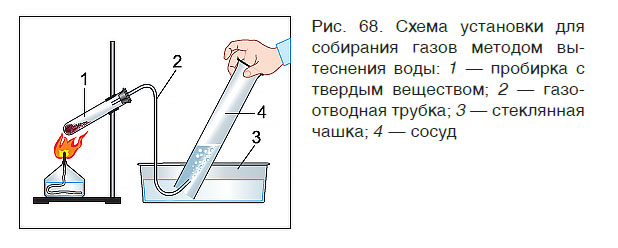
В лабораторных условиях собрать газ в сосуд можно двумя способами: вытеснением воды (рис. 68) и вытеснением воздуха. Первый способ применяют для собирания только нерастворимых в воде газов (кислород, азот, водород). Вто-
рой — для собирания как растворимых (аммиак, углекислый газ), так и нерастворимых в воде газов.
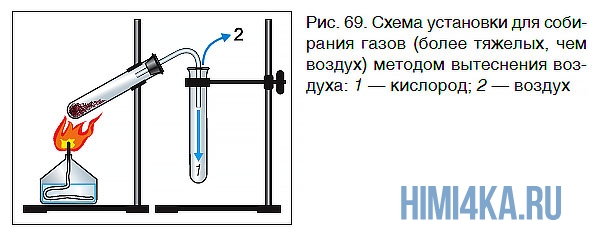
Для собирания газов, которые легче воздуха, сосуд для сбора газа следует закрепить дном вверх, а для газов, которые тяжелее воздуха, — дном вниз (рис. 69)
Для хранения газов следует использовать сосуды, не сообщающиеся с окружающей средой. Такие сосуды называют герметичными (т. е. не имеющими отверстий для выхода газа из сосуда наружу). В быту примером герметичного сосуда является бутылка с плотной пробкой, завязанный воздушный шарик или накачанная камера от велосипедного колеса, в химической лаборатории — пробирка, плотно закрытая пробкой, газометр.
Из курса физики вы знаете, что при нагревании газы расширяются. Это свойство можно использовать для проверки прибора для получения газов на герметичность (рис. 70). Для этого после сборки прибора следует погрузить конец газоотводной трубки в воду, а пробирку на несколько секунд зажать в ладони. Нагреваясь от тепла руки, воздух в пробирке расширяется и выходит из газоотводной трубки в виде пузырьков. Если пузырьки не наблюдаются, то это свидетельствует о том, что прибор собран негерметично и для газа имеется другой выход, кроме газоотводной трубки.
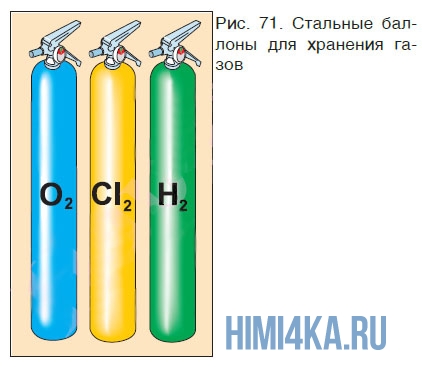
В промышленности для хранения газов чаще всего используют более прочные сосуды — баллоны (рис. 71), в которых сжатые газы находятся под большим давлением; для предупреждения разрушения баллона сжатым газом его стенки делают из толстой стали. Узнать, какой газ содержится в баллоне, можно по окраске баллона, цвету надписи на нем и цвету полосы. Например, баллон с кислородом должен быть окрашен в голубой цвет и иметь черную надпись «Кислород», баллон с азотом должен быть окрашен в черный цвет, иметь желтую надпись «Азот» и коричневую полосу, баллон с очень чистым аргоном должен быть окрашен в серый цвет, иметь зеленую надпись «Аргон» и зеленую полосу.
Краткие выводы урока:
- Вещества могут находиться в газообразном, жидком или твердом агрегатном состоянии.
- Воздух представляет собой смесь газов. Основными компонентами воздуха являются азот и кислород.
- При нормальных условиях в воздухе объемом 100 дм3 содержится азот объемом около 78 дм3 и кислород объемом около 21 дм3.
- Воздух можно условно рассматривать как газ, молярная масса которого равна 29 г/моль.
Надеюсь урок 15 «Воздух как смесь газов» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.