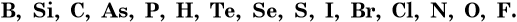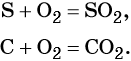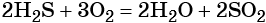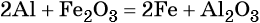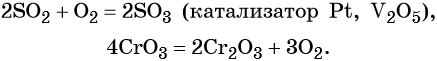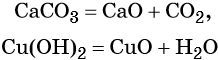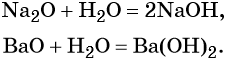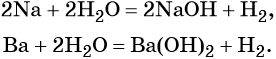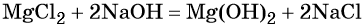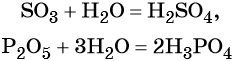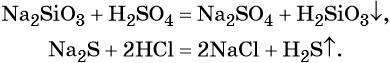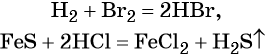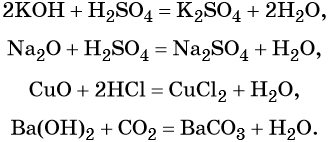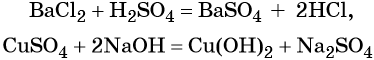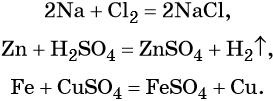Атомы и молекулы. Химический элемент. Простые и сложные вещества. Основные классы неорганических веществ. Номенклатура неорганических соединений

Атом — электронейтральная частица, состоящая из положительно заряженного ядра и отрицательно заряженных электронов.
Молекулой называют наименьшую электронейтральную частицу вещества, способную к самостоятельному существованию и обладающую его химическими свойствами. Молекула представляет собой систему взаимодействующих между собой атомов, образующих определённую структуру с помощью химических связей.
Химический элемент — совокупность атомов, характеризующихся одинаковым значением (величиной) заряда ядра.
Ионами называют электрически заряженные частицы, возникающие при потере или присоединении электронов атомами или молекулами.
Катионами называют положительно заряженные ионы.
Анионами называют отрицательно заряженные ионы.
Вещество — любая совокупность атомов и молекул.
Свойства веществ (температуры плавления и кипения, плотность, цвет и т. д.) относятся к совокупности атомов или молекул.
По химическому составу неорганические вещества делят на простые и сложные.
Простыми называют вещества, которые образуют атомы одного и того же химического элемента (например, H2, O2).
Простые вещества делят на металлы и неметаллы.
Металлами называют простые вещества, которые обладают характерными металлическими свойствами, а именно высокой электро- и теплопроводностью и металлическим блеском.
Простые вещества, которые образуют атомы элементов-неметаллов, при нормальных условиях такими свойствами не обладают.
В периодической таблице Д.И. Менделеева неметаллы расположены в главных подгруппах справа вверху от условной диагонали, проведённой через бор и астат. В главных подгруппах слева от этой диагонали и во всех побочных подгруппах располагаются металлы.
Сложными называют вещества, которые состоят из атомов двух и более элементов (например, H2S, NO2).
Для выражения состава вещества используют различные химические формулы. При их написании используют общепринятые символы химических элементов. Символ элемента состоит из первой буквы или первой и одной из последующих букв латинского названия элемента, при этом первая буква всегда прописная, а вторая — строчная.
Названия и обозначения атомов совпадают с символами химических элементов. Например, О — атом кислорода, 2О — два атома кислорода, О2 — молекула кислорода, О3 — молекула озона.
Сложные вещества разделяют на условно электроположительную (катион) и условно электроотрицательную (анион) составляющие. В формуле сложного вещества вначале ставят катион, а затем — анион, например KBr, CuSO4. Названия сложного вещества читают справа налево, т. е. вначале называют его электроотрицательную составляющую в именительном падеже, а затем электроположительную в родительном падеже.
Для бинарных, т. е. состоящих из двух элементов соединений, действуют следующие правила. Если соединение состоит из металла и неметалла, то на первом месте всегда ставят металл (как более электроположительный элемент): K2S, BaCl2.
В формулах соединений, состоящих только из неметаллов, на первом месте всегда ставят элемент, находящийся левее в условном ряду неметаллов, построенном по их возрастающей электроотрицательности:
Например, IBr — бромид йода, CS2 — дисульфид углерода.
Формула молекулярная (брутто-формула) включает символы всех химических элементов, входящих в состав соединений. Около каждого символа ставят числовой индекс, показывающий, сколько атомов данного вида входит в состав соединения. Таким образом, молекулярная формула показывает качественный и количественный состав молекулы. Например, формула KNO3 показывает, что вещество состоит из 1 атома калия (индекс, равный 1, не ставится), 1 атома азота и 3 атомов кислорода.
Чтобы правильно прочитать формулу, надо знать как русские, так и латинские обозначения элементов. Называя вещество «вода», мы говорим, что его формула H2O (читается «аш два о»). Данное вещество состоит из двух атомов водорода и одного атома кислорода.
Называя вещество сульфат калия, K2SO4, мы читаем его формулу «калий два эс о четыре». Данное вещество состоит из двух атомов калия, одного атома серы и четырех атомов кислорода.
Если в формуле структурный фрагмент повторяется несколько раз, его заключают в круглые скобки и за скобками ставят числовой индекс, который произносят «дважды», «трижды», например, Ca(NO3)2 читается «кальций эн о три дважды», Mg3(PO4)2 читается «магний три пэ о четыре дважды».
Коэффициент, стоящий перед формулой вещества в уравнении реакции, читают как число, например: 3HNO2 — «три аш эн о два».
Оксидами называют класс химических соединений, состоящий из какого-либо элемента и атома кислорода со степенью окисления –2.
Называют оксиды, руководствуясь следующими правилами:
- Вначале указывают слово оксид, а затем в родительном падеже название второго элемента;
- Если элемент может образовать несколько оксидов, то после названия элемента в скобках указывают его валентность;
- При написании формул оксидов кислород всегда ставят на втором месте.
Примеры: K2O — оксид калия, N2O5 — оксид азота (V), CrO3 — оксид хрома (IV).
Для некоторых распространённых оксидов используют тривиальные названия, например CaO — негашеная известь, N2O — веселящий газ, CO — угарный газ, CO2 — углекислый газ.
Оксиды классифицируют так.
Низшими называют оксиды, в которых элемент проявляет низшую степень окисления, например MnO — оксид марганца (II).
Высшими называют оксиды, в которых элемент проявляет высшую степень окисления, например Mn2O7 — оксид марганца (VII).
Несолеобразующими, или безразличными, называют оксиды, не проявляющие ни основные, ни кислотные свойства, например N2O, NO, CO.
Солеобразующими называют группу кислотных, основных и амфотерных оксидов.
Кислотные оксиды образуют неметаллы и некоторые металлы в высших степенях окисления. Примеры кислотных оксидов: CO2, SiO2, N2O3, NO2, N2O5, P2O3, P2O5, SO2, SO3, Cl2O5, Cl2O7, CrO3, Mn2O7.
Основные оксиды образуют металлы в низших степенях окисления. Наиболее известные из них: Li2O, Na2O, K2O, Rb2O, Cs2O, MgO, CaO, SrO, BaO, Cu2O, Ag2O, HgO, CrO, FeO.
Амфотерными называют оксиды, которые проявляют как основные, так и кислотные свойства, в зависимости от другого реагента. Наиболее известные амфотерные оксиды Al2O3, Cr2O3, ZnO, BeO, PbO, SnO. Ряд оксидов, например CuО, Fe2O3, проявляет амфотерные свойства с преобладанием основных.
Существует несколько способов получения оксидов.
Реакции простых веществ с кислородом:
При взаимодействии сложных веществ с кислородом часто образуется смесь оксидов элементов:
Оксиды металлов реагируют с химически более активными металлами. При этом образуется новый оксид и новый металл:
Некоторые высшие оксиды получают доокислением низших оксидов, а ряд низших оксидов получают разложением высших оксидов:
Иногда для получения оксидов используют реакции разложения солей и гидроксидов:
Основаниями называют класс химических соединений, которые состоят из катиона металла или иона аммония и одной или нескольких гидроксильных групп, способных к замещению на анионы.
Число гидроксильных групп определяет кислотность основания, например: NaOH — однокислотное, Mg(OH)2 — двухкислотное и т. д.
Щелочами называют растворимые в воде основания.
Сильные основания: гидроксиды щелочных и щёлочноземельных металлов LiOH, NaOH, KOH, RbOH, CsOH, Ba(OH)2, Ca(OH)2, Sr(OH)2. Слабые основания: все нерастворимые в воде гидроксиды металлов и гидрат аммиака.
Называют основания следующим образом:
- Вначале указывают слово гидроксид, а затем добавляют название металла в родительном падеже;
- Если элемент может образовывать несколько оснований, то после его названия в круглых скобках римской цифрой указывают валентность: KOH — гидроксид калия, Fe(OH)2 — гидроксид железа (II), Fe(OH)3 — гидроксид железа (III);
- При написании формул гидроксидов гидроксильную группу всегда ставят на втором месте.
Для некоторых распространённых гидрокидов используют тривиальные названия, например: Ca(OH)2 — гашёная известь; NaOH — едкий натр, или каустик.
Существуют следующие способы получения оснований:
Реакция основных оксидов с водой:
Взаимодействие некоторых металлов с водой:
Реакция обмена между солями и основаниями:
Первые два способа применяют для получения растворимых, а последний — для получения нерастворимых в воде оснований. Существуют и иные способы получения оснований.
Все растворы щелочей имеют pH > 7. При этих значениях pH происходит изменение окраски индикаторов: лакмуса — на синюю, фенолфталеина — на малиновую, метилового оранжевого — на жёлтую, что является качественным методом обнаружения щелочей. Более подробный материал о показателе pH будет изложен в уроке 24.
Кислотами называют класс химических соединений, которые содержат в своём составе один или несколько катионов водорода, способных замещаться на атомы металлов, и анионов кислотных остатков.
Основностью кислоты называют число способных замещаться на металл атомов водорода в её молекуле. По основности кислоты делят на одно-, двух- и трёхосновные, например HBr, H2S и H3PO4 соответственно.
В зависимости от элементного состава кислоты делят на бескислородные и кислородные, например HBr и H2SO3. Кислотный остаток — это структурный элемент молекулы кислоты, который выступает как единое целое в ходе химических реакций.
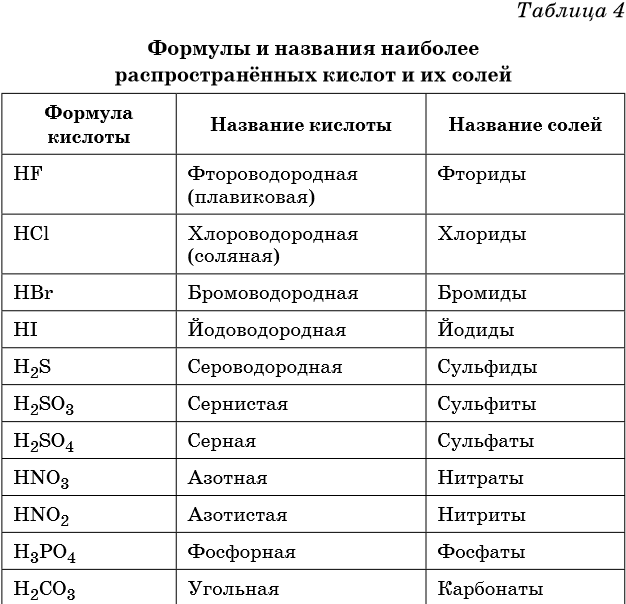
В таблице 4 приведены формулы и названия наиболее распространенных кислот и их солей.
Сильные кислоты: HI, HBr, HCl, HClO3, HClO4, H2SO4, HNO3.
Кислоты средней силы: H2SO3, H3PO4, HF, HNO2.
Слабые кислоты: CH3COOH, H2CO3, H2S, H2SiO3.
Кислородсодержащие кислоты и основания объединяют в общий класс гидроксидов.
Амфотерными называют гидроксиды, способные реагировать как с кислотами, так и с основаниями. Амфотерные гидроксиды: Al(OH)3, Cr(OH)3, Zn(OH)2, Pb(OH)2, Be(OH)2, Sn(OH)2. Некоторые гидроксиды, например Cu(OH)2, Fe(OH)3, проявляют амфотерные свойства с преобладанием основных.
Большинство кислородных кислот получают реакцией соответствующих оксидов с водой:
Некоторые кислоты получают из солей путём вытеснения более сильной кислотой, например:
Бескислородные кислоты получают прямым взаимодействием неметалла с водородом либо действием более сильных кислот на соответствующие соли:
При обычных условиях кислоты представляют собой жидкости (HNO3, H2SO4), твёрдые (H3PO4) и газообразные (HCl) вещества. Большая часть кислот смешиваются с водой в любых соотношениях. Водные растворы кислот имеют pH < 7. При этих значениях pH индикаторы имеют следующую окраску: лакмус — красную, метиловый оранжевый — розовую. Водные растворы кислот имеют кислый вкус и разъедают растительные и животные ткани.
Солями называют класс химических соединений, которые представляют собой продукты взаимодействия кислот с основаниями.
По составу соли классифицируют на средние, кислые и основные.
Средними называют соли, которые состоят только из катиона металла или иона аммония и аниона кислотного остатка, например: CsBr, MgSO4.
Кислыми называют соли, которые наряду с катионом металла содержат катионы водорода, способные замещаться на другие катионы в ходе обменных реакций, например: LiHCO3 (гидрокарбонат лития), CaHPO4 (гидрофосфат кальция).
Основными называют соли, которые наряду с анионом кислотного остатка содержат одну или несколько гидроксильных групп, способных замещаться на анионы в ходе реакций обмена, например: Al(OH)2Br, Cu(OH)I.
При написании формул солей на первом месте ставят катион, а при написании названий — анион. Названия солей состоят из названия аниона в именительном падеже и названия катиона в родительном. Например, NaBr — бромид натрия, BaCO3 — карбонат бария. Если металл проявляет различные степени окисления, то в названиях степень окисления указывается римской цифрой: FeCl2 — хлорид железа (II), FeCl3 — хлорид железа (III). Кислые соли называют добавлением к аниону приставки гидро-, а если необходимо, то и соответствующего числительного, например: NaHCO3 — гидрокарбонат натрия, КH2PO4 — дигидрофосфат калия, Al(OH)2Br — дигидроксобромид алюминия, Cu(OH)I — гидроксойодид меди (II).
Основные соли называют добавлением приставки гидроксо- к названию кислотного остатка, указывая, если необходимо, соответствующее числительное: Mg(OH)Cl — гидроксохлорид магния, Al(OH)2Cl — дигидроксохлорид алюминия.
Существует множество путей получения солей. Приведём наиболее важные из них.
Реакция нейтрализации, т. е. взаимодействие кислот и оснований, взаимодействие кислот с основными и амфотерными оксидами и реакция оснований с кислотными оксидами:
Взаимодействие кислот или щелочей с солями:
Взаимодействие металлов с неметаллами, кислотами, солями:
Взаимодействие основных и кислотных оксидов:
По своим физическим свойствам соли — твёрдые кристаллические вещества, часто имеющие высокие температуры плавления. По растворимости в воде соли делятся на растворимые (более 1 г вещества на 100 г воды), малорастворимые (от 0,1 до 1 г вещества на 100 г воды) и нерастворимые (менее 0,1 г вещества на 100 г воды). В воде растворимы все соли азотной и уксусной кислот.
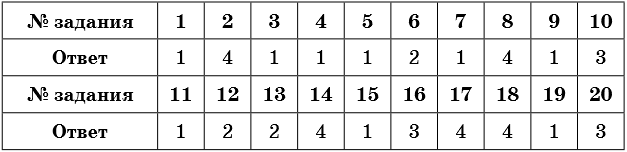
Тренировочные задания
1. Кислотой и амфотерным гидроксидом соответственно являются
1) H2SO4 и Zn(OH)2
2) Ca(OH)2 и HCl
3) HF и Cr2O3
4) Al(OH)3 и HNO3
2. Основанием и кислотным оксидом соответственно являются
1) Al(OH)3 и Cr2O3
2) H2SO4 и N2O
3) NaOH и Al2O3
4) Sr(OH)2 и N2O3
3. Кислой солью и несолеобразующим оксидом соответственно являются
1) NaHSO4 и N2O
2) Ba(HCO3)2 и FeO
3) NaHS и Cr2O3
4) AlCl3 и NO
4. Гидроксидом и щёлочью соответственно являются
1) H3PO4 и KOH
2) Ba(OH)2 и HBr
3) Fe(OH)3 и Fe(OH)2
4) Al(OH)3 и Ca(OH)2
5. Вещество, химическая формула которого Cr2(SO4)3, имеет название
1) сульфат хрома (III)
2) сульфит хрома (III)
3) сульфат хрома (II)
4) сульфит хрома (II)
6. Вещество, химическая формула которого CaHPO4, называется
1) фосфат кальция
2) гидрофосфат кальция
3) дигидрофосфат кальция
4) фосфид кальция
7. К простым веществам относится
1) поваренная соль
2) кислород
3) оксид кремния
4) пищевая сода
8. К простым веществам относится
1) поташ
2) углекислый газ
3) веселящий газ
4) бром
9. К сложным веществам относится
1) поташ
2) сера
3) озон
4) бром
10. К сложным веществам относится
1) фтор
2) фосфор
3) углекислый газ
4) бром
11. Только основные оксиды приведены в списке
1) Li2O, MgO, Ag2O
2) N2O, MgO, CuO
3) Cr2O3, MgO, Na2O
4) FeO, MgO, ZnO
12. Только несолеобразующие оксиды приведены в списке
1) CrO, CO, K2O
2) N2O, NO, CO
3) CrO3, SO2, Li2O
4) N2O3, MgO, P2O3
13. В перечне веществ, формулы которых: А) H2O В) HNO3 Д) CaO Б) N2O Г) H2SO4 Е) NaOH к оксидам относятся
1) АБВ
2) АБД
3) БВД
4) БДЕ
14. В перечне веществ, формулы которых: А) CaO В) Cr2O3 Д) SrO Б) Fe2O3 Г) NO Е) Li2O к основным оксидам относятся
1) АБВ
2) АБД
3) БВД
4) АДЕ
15. В перечне веществ, формулы которых: А) CO2 В) SO2 Д) SrO Б) CrO3 Г) Cr2O3 Е) CrO к кислотным оксидам относятся
1) АБВ
2) АБД
3) БВД
4) АДЕ
16. В перечне веществ, формулы которых: А) CrO В) ZnO Д) Al2O3 Б) CrO3 Г) Cr2O3 Е) NO к амфотерным оксидам относятся
1) АБВ
2) АВД
3) ВГД
4) АДЕ
17. В перечне веществ, формулы которых: А) NH4Cl В) (NH4)2HPO4 Д) Ca3(PO4)2 Б) NH4NO3 Г) NH4HSO4 Е) Ca(HCO3)2 к средним солям относятся
1) АБВ
2) БВГ
3) БВД
4) АБД
18. В перечне веществ, формулы которых: А) HCl В) (NH4)2HPO4 Д) H3PO4 Б) HNO3 Г) NH4HSO4 Е) Ca(HCO3)2 к кислотам относятся
1) АБВ
2) БВГ
3) БВД
4) АБД
19. Только сильные кислоты приведены в списке
1) HI, HClO3, HNO3
2) H2S, HI, HClO4
3) CH3COOH, H2CO3, H2S
4) HCl, HF, HBr
20. Только слабые кислоты приведены в списке
1) HI, HClO3, HNO2
2) H2SO3, HNO2, H3PO4
3) CH3COOH, H2CO3, H2SiO3
4) HCl, HF, HBr