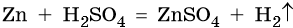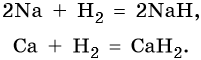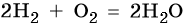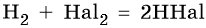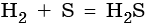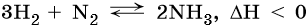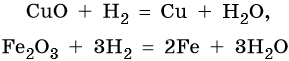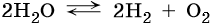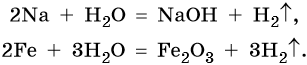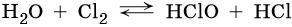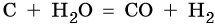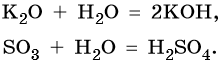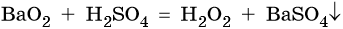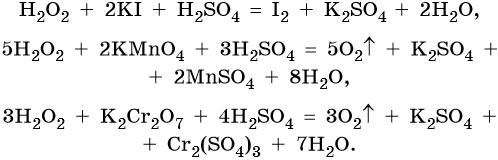Водород

Водород занимает особое положение в Периодической системе химических элементов Д.И. Менделеева. По числу валентных электронов, способности образовывать в растворах гидратный ион H+ он сходен со щелочными металлами, и его следует поместить в I группу. По числу электронов, необходимых для завершения внешней электронной оболочки, значению энергии ионизации, способности проявлять отрицательную степень окисления, малому атомному радиусу водород следует поместить в VII группу периодической системы. Таким образом, размещение водорода в той или иной группе периодической системы в значительной мере условно, но в большинстве случаев его помещают в VII группу.
Электронная формула водорода 1s1. Единственный валентный электрон находится непосредственно в сфере действия атомного ядра. Простота электронной конфигурации водорода отнюдь не означает, что химические свойства этого элемента просты. Напротив, химия водорода во многом отличается от химии других элементов. Водород в своих соединениях способен проявлять степени окисления +1 и –1.
Существует большое количество методов получения водорода. В лаборатории его получают взаимодействием некоторых металлов с кислотами, например:
Водород можно получить электролизом водных растворов серной кислоты или щелочей. При этом происходит процесс выделения водорода на катоде и кислорода на аноде.
В промышленности водород получают главным образом из природных и попутных газов, продуктов газификации топлива и коксового газа.
Простое вещество водород (H2) представляет собой горючий газ без цвета и запаха. Температура кипения –252,8 °C. Водород в 14,5 раз легче воздуха, мало растворим в воде.
Молекула водорода устойчива, обладает большой прочностью. Из-за высокой энергии диссоциации (435 кДж/моль) распад молекул H2 на атомы происходит в заметной степени лишь при температуре выше 2000 °C.
Для водорода возможны положительная и отрицательная степени окисления, поэтому в химических реакциях водород может проявлять как окислительные, так и восстановительные свойства. В тех случаях, когда водород выступает в качестве окислителя, он ведет себя подобно галогенам, образуя аналогичные галогенидам гидриды (гидридами называют группу химических соединений водорода с металлами и менее электроотрицательными, чем он, элементами):
По окислительной активности водород существенно уступает галогенам. Поэтому ионный характер проявляют лишь гидриды щелочных и щелочноземельных металлов. Ионные, а также комплексные гидриды, например, являются сильными восстановителями. Их широко используют в химических синтезах.
В большинстве реакций водород ведет себя как восстановитель. При нормальных условиях водород не взаимодействует с кислородом, однако при поджигании реакция протекает со взрывом:
Смесь двух объемов водорода с одним объемом кислорода называют гремучим газом. При контролируемом горении происходит выделение большого количества тепла, и температура водородно-кислородного пламени достигает 3000 °C.
Реакция с галогенами протекает, в зависимости от природы галогена, по-разному:
С фтором такая реакция идет со взрывом даже при низких температурах. С хлором на свету реакция также протекает со взрывом. С бромом реакция идет значительно медленнее, а с йодом не доходит до конца даже при высокой температуре. Механизм этих реакций радикальный.
При повышенной температуре водород взаимодействует с элементами VI группы — серой, селеном, теллуром, например:
Очень важной является реакция водорода с азотом. Эта реакция обратима. Для смещения равновесия в сторону образования аммиака используют повышенное давление. В промышленности данный процесс осуществляют при температуре 450–500 °C в присутствии различных катализаторов:
Водород восстанавливает многие металлы из оксидов, например:
Данную реакцию используют для получения некоторых чистых металлов.
Огромную роль играют реакции гидрирования органических соединений, которые широко используют как в лабораторной практике, так и в промышленном органическом синтезе.
Сокращение природных источников углеводородного сырья, загрязнение окружающей среды продуктами сгорания топлива повышают интерес к водороду как к экологически чистому топливу. Вероятно, водород будет играть важную роль в энергетике будущего.
В настоящее время водород широко применяют в промышленности для синтеза аммиака, метанола, гидрогенизации твердого и жидкого топлива, в органическом синтезе, для сварки и резки металлов и т. д.
Вода H2O, оксид водорода, является важнейшим химическим соединением. При нормальных условиях вода — бесцветная жидкость, без запаха и вкуса. Вода — самое распространенное вещество на поверхности Земли. В человеческом организме содержится 63–68% воды.
Физические свойства воды во многом являются аномальными. При нормальном атмосферном давлении вода кипит при 100 °C. Температура замерзания чистой воды 0 °C. B отличие от других жидкостей плотность воды при охлаждении возрастает не монотонно, а имеет максимум при +4 °C. Теплоемкость воды очень высока и составляет 418 кДж/моль·K. Теплоемкость льда при 0 °C составляет 2,038 кДж/моль·K. Аномально высокой является теплота плавления льда. Электропроводность воды очень мала. Аномальные физические свойства воды объясняют ее строение. Валентный угол H–O–H равен 104,5°. Молекула воды представляет собой искаженный тетраэдр, в двух вершинах которого располагаются атомы водорода, а две другие заняты орбиталями неподеленных пар электронов атома кислорода, не участвующих в образовании химических связей.
Вода является стабильным соединением, ее разложение на кислород и водород происходит лишь под действием постоянного электрического тока или при температуре около 2000 °C:
Вода непосредственно взаимодействует с металлами, стоящими в ряду стандартных электронных потенциалов до водорода. Продуктами реакции в зависимости от природы металла могут быть соответствующие гидроксиды и оксиды. Скорость реакции в зависимости от природы металла также изменяется в широких пределах. Так, натрий вступает в реакцию водой уже при комнатной температуре, реакция сопровождается выделением большого количества тепла; железо реагирует с водой при температуре 800 °С:
Вода может вступать в реакцию со многими неметаллами. Так, при обычных условиях вода обратимо взаимодействует с хлором:
При повышенной температуре вода взаимодействует с углем с образованием так называемого синтез-газа — смеси оксида углерода (II) и водорода:
При обычных условиях вода реагирует со многими основными и кислотными оксидами с образованием оснований и кислот соответственно:
Реакция идет до конца, если соответствующее основание или кислота растворимы в воде.
Пероксид водорода (H2O2) представляет собой бесцветную жидкость, очень неустойчивую при комнатной температуре. Концентрированные растворы пероксида водорода взрывоопасны. В лаборатории H2O2 получают с помощью обменной реакции между пероксидом бария и концентрированной серной кислотой:
В химических реакциях H2O2 может проявлять свойства как окислителя, так и восстановителя, например: