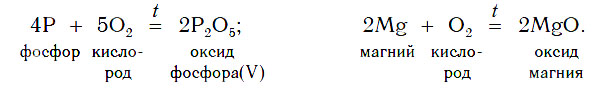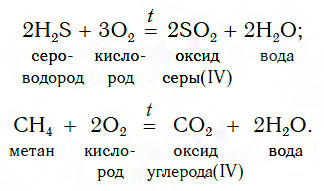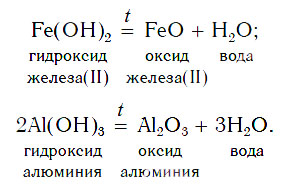Урок 33. Получение и применение оксидов
В уроке 33 «Получение и применение оксидов» из курса «Химия для чайников» узнаем как получать оксиды различными способами, а также познакомимся с широким спектром применения оксидов во всех отраслях промышленности и быта.
Получение оксидов
1. Взаимодействие простых веществ с кислородом
Некоторые оксиды образуются в результате сжигания в кислороде (или на воздухе) соответствующих простых веществ. Так можно получить оксиды углерода(IV), серы(IV), фосфора(V), магния и других неметаллов и металлов:
2. Взаимодействие сложных веществ с кислородом
Оксиды можно получать также сжиганием в кислороде (или на воздухе) некоторых сложных веществ, например:
3. Термическое разложение нерастворимых оснований
Применение оксидов
Один из наиболее широко использующихся оксидов — вода H2O, о применении которой в быту, технике и ромышленности вы уже знаете.
Разнообразное применение находят и некоторые другие оксиды. Так, например, из оксида железа(III) Fe2O3, входящего в состав железных руд, в промышленности получают железо, а из оксида алюминия Al2O3 — алюминий. Оксид алюминия применяют также для изготовления искусственных драгоценных камней — рубина и сапфира. Мелкие кристаллы этого оксида применяются также в производстве наждачной бумаги.
Оксид углерода(IV) (углекислый газ) используют в пищевой промышленности для изготовления всех газированных напитков, для увеличения срока сохранности фруктов и овощей. Этим веществом наполняют углекислотные огнетушители. Твердый оксид углерода(IV) под названием «сухой лед» (рис. 117) применяют для хранения мороженого, для сильного охлаждения различных материалов.
Достаточно широко используется и оксид серы(IV) SO2 (сернистый газ). Он находит применение в производстве серной кислоты, для дезинфекции складских помещений, уничтожения вредных насекомых и бактерий, отбеливания бумаги.
Оксид кремния(IV) SiO2 в виде кварцевого песка используется в производстве стекла и бетона. Вместе с оксидом свинца(II) PbO он применяется для изготовления полудрагоценных камней и украшений («кристаллы Сваровски»).
Оксид кальция СaO под названием «негашеная известь» применяют при изготовлении различных строительных материалов. Оксиды некоторых других металлов находят применение в производстве красок. Так, например, Fe2O3 используют для изготовления краски коричневого, Сr2O3 — зеленого, ZnO и TiO2 — белого цветов.
Краткие выводы урока:
- Оксиды образуются при взаимодействии кислорода с простыми и сложными веществами.
- Оксиды можно получить термическим разложением нерастворимых оснований.
- Оксиды находят широкое практическое применение в промышленности и в быту.
- Оксиды — вода H2O и углекислый газ СО2 — участвуют в процессе фотосинтеза.
Надеюсь урок 33 «Получение и применение оксидов» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии. Если вопросов нет, то переходите к следующему уроку.