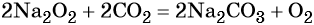Человек в мире веществ, материалов и химических реакций

Как отмечалось ранее, в процессе жизнедеятельности человеческого организма реализуется около миллиона различных химических процессов. В любой живой клетке человеческого организма могут протекать тысячи химических реакций.
Понимание химических процессов, лежащих в основе болезни, помогает поиску способов её лечения. Основоположником медицинского направления в химии был швейцарский врач Т. Парацельс. Именно ему принадлежит высказывание, что цель химии состоит не в изготовлении золота и серебра, а в изготовлении лекарств. Парацельс впервые стал систематически применять для лечения больных неорганические вещества.
В результате естественного отбора основу живых организмов составляют только шесть элементов. Это углерод, водород, кислород, азот, фосфор и сера. Их общее групповое название — органогены. Человеческий организм на 97,4% состоит из органогенов.
Жизненно необходимыми (незаменимыми) элементами являются водород, кислород, азот, фосфор, сера, натрий, калий, магний, кальций, хлор, йод, марганец, медь, кобальт, железо, цинк, молибден и ванадий. Они постоянно содержатся в организме. Их дефицит приводит к нарушению нормальной жизнедеятельности человека.
Ниже приведены сведения о некоторых практически значимых и биологически активных неорганических веществах, которые носят прежде всего справочный характер. Сведения об элементах и их соединениях приведены в соответствии с их расположением в таблице Д.И. Менделеева.
Содержание
- Натрий и его соединения
- Калий и его соединения
- Магний и его соединения
- Кальций и его соединения
- Алюминий и его соединения
- Углерод и его соединения
- Кремний и его соединения
- Азот и его соединения
- Фосфор и его соединения
- Кислород и его соединения
- Сера и её соединения
- Фтор и его соединения
- Хлор и его соединения
- Бром и его соединения
- Йод и его соединения
- Железо и его соединения
- Тренировочные задания
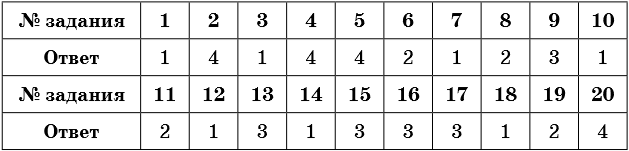
- Ответы
Натрий и его соединения
Гидроксид натрия применяют в качестве реагента в химической промышленности, в производстве бумаги, искусственных волокон, для очистки нефти, масел и т. д.
В практике широко используют следующие соединения натрия.
Пероксид натрия Na2O2, используют для отбеливания различных материалов, для регенерации кислорода в дыхательных приборах изолирующего типа по реакции:
Карбонат и гидрокарбонат натрия Na2CO3 и NaHCO3 относятся к многотоннажным продуктам химической промышленности, применяются в различных отраслях химической, мыловаренной, бумажной, текстильной и пищевой промышленности.
Нитрат натрия NaNO3 применяют как удобрение, в производстве стекла, как консервант пищевых продуктов и т. д.
Хлорид натрия NaCl (поваренная соль) применяют в технике, пищевой промышленности и т. д.
Натрий относится к жизненно важным элементам. Он распределён по всему организму и является основным внеклеточным ионом. Ион натрия участвует в регуляции водного обмена и влияет на работу ферментов.
В медицине применяют растворы хлорида натрия различной концентрации для инъекций, промывания ран, компрессов и т. д. Кроме того, в медицине применяют питьевую соду NaHCO3 при различных заболеваниях, сопровождающихся повышенной кислотностью, а также бромид натрия как седативное средство и иодид натрия при лечении зоба.
Калий и его соединения
Гидроксид калия применяют для получения мыла, в щелочных аккумуляторах, как поглотитель кислых газов и т. д.
Около 90% добываемых солей калия потребляются в качестве удобрений.
Калий ускоряет процесс фотосинтеза и содействует накоплению углеводов в растениях. В качестве калийных удобрений используют природные (сырые) калийные соли и промышленные концентрированные удобрения.
Концентрированными удобрениями являются хлорид и сульфат калия.
Хлорат калия KClO3 (бертолетова соль) и нитрат калия KNO3 используют в пиротехнике.
Катион K+ является основным внутриклеточным катионом. Этот катион играет важную роль в нормальном функционировании сердца, проведении нервных импульсов, активизации ферментов.
В медицинской практике применяют хлорид калия при калиевом истощении, бромид калия KBr как седативное средство, а также некоторые другие соединения калия.
Магний и его соединения
Магний в основном используют для производства «сверхлёгких» сплавов. Одним из наиболее важных является сплав электрон, который применяют в ракетной технике и авиастроении. Кроме того, магний используют в металлотермии, при изготовлении осветительных и зажигательных ракет, снарядов и т. д.
Магний играет важную роль в жизнедеятельности живых организмов и человека. В медицинской практике используют оксид магния при избыточной кислотности, а также сульфат магния MgSO4 × 7H2O в качестве слабительного и желчегонного средства.
Кальций и его соединения
Гидроксид кальция Ca(OH)2 (известковое молоко, гашеная известь) — белое кристаллическое вещество, плохо растворимое в воде. Получают его из соответствующего оксида. Является сильным основанием. Применяют как вяжущий материал в строительстве, для раскисления почв, в производстве стекла, сахара и т. д.
Природные соединения кальция широко применяют в производстве вяжущих материалов. Вяжущими материалами называют порошкообразные вещества, образующие при смешении с водой пластичную массу, затвердевающую в твёрдое камневидное тело. Их широко используют для изготовления бетона, строительных деталей и конструкций, а также для сцепления отдельных элементов сооружений. К вяжущим веществам относятся цементы, гипсовые материалы, известь и др.
Кальций играет исключительно важную роль в жизнедеятельности человеческого организма. Катион Ca2+ присутствует в каждой клетке человеческого организма, а основная его масса сосредоточена в костной и зубной ткани в виде нерастворимого кристаллического минерала — гидроксилапатита Ca10(PO4)6(OH)2. Ионы кальция принимают активное участие в сокращении мышц, передаче нервных импульсов и т. д.
В медицинской практике широко применяют ряд препаратов, являющихся кальциевыми солями различных органических кислот: глутаминовой, молочной и т. д. Из используемых в медицине неорганических солей кальция наиболее известен жжёный гипс CaSO4 × ½H2O (гипсовые повязки при переломах), а также хлорид кальция.
Алюминий и его соединения
Алюминий широко применяют как конструкционный материал, основу для создания лёгких сплавов (например, дюралюминий; силумин). Сплавы алюминия используются в авиастроении, автомобилестроении и судостроении. Из алюминия изготавливают электрические провода, алюминиевую фольгу используют в пищевой промышленности.
Из солей алюминия отметим его сульфат Al2(SO4)3 и алюминиевые квасцы общей формулы MAl2(SO4)3 × 12H2O, где М = K, NH4, Na. Так, алюмо-калиевые квасцы KAl(SO4)2 × 12H2O используют как дубитель, протраву при крашении, для проклейки бумаги и т. д.
Биологическая роль алюминия выяснена недостаточно подробно. Известно, что алюминий влияет на развитие эпителиальной и соединительной ткани, ряд ферментативных процессов и т. д.
В медицинской практике применяют гидроксид алюминия и различные препараты на его основе в качестве обволакивающих, абсорбирующих и антацидных средств. Алюмо-калиевые квасцы применяют как кровоостанавливающее средство.
Углерод и его соединения
Их широко используют во всех отраслях промышленности. Так, алмаз применяют для обработки особо твердых материалов, при буровых работах. Кристаллы алмаза после огранки и шлифования называются бриллиантами и применяются для изготовления ювелирных изделий.
Графит используют для приготовления электродов, плавильных тиглей, в качестве замедлителя нейтронов в атомных реакторах, для изготовления карандашей, как смазочный материал и т. д.
Технические сорта графита: кокс, древесный уголь, животный уголь — сажу используют в металлургии, для изготовления красок, чёрной резины, в качестве адсорбентов и т. д.
Углерод является органогеном. На его основе построены все органические соединения. Он входит в состав тканей и клеток в форме белков, жиров, углеводов, витаминов и гормонов.
В медицинской практике при различных отравлениях применяют специально обработанный уголь животного или растительного происхождения, так называемый активированный уголь.
Кремний и его соединения
Их широко применяют в технике как основу полупроводниковых материалов, как легирующие добавки к сталям и т. д.
Карбид кремния SiC (карборунд) применяют как абразивный и огнеупорный материал, в радиотехнике и т. д.
Нитрид кремния Si3N4 используют в качестве химически стойкого и огнеупорного материала, в создании тугоплавких сплавов, в качестве высокотемпературного полупроводника.
Огромный научный интерес представляют кремнийорганические соединения.
Биологическая роль кремния выяснена недостаточно. Убедительных данных о заболеваниях, вызванных недостатком кремния, нет.
Вдыхание пыли, содержащей SiO2, приводит к силикозу.
В медицинской практике применяют карбид кремния SiC для шлифовки пломб и пластмассовых протезов.
Азот и его соединения
Нитраты широко используются в производстве легко воспламеняющихся и взрывчатых веществ. Так, черный порох имеет следующий состав: 68% KNO3, 15% S, 17% С.
Азотную кислоту широко используют в производстве взрывчатых веществ, искусственных волокон и пластических масс, для травления металлов, в ракетной технике.
Особую роль играют азотные удобрения, которые очень широко применяются в сельском хозяйстве. Из них отметим нитрат натрия NaNO3, нитрат калия KNO3, нитрат аммония NH4NO3, сульфат аммония (NH4)2SO4 и карбамид (мочевину) OC(NH2)2.
Азот является органогеном. Он входит в состав всех важнейших органических соединений. В медицинской практике применяют 10%-ный раствор NH3 как средство скорой помощи для возбуждения дыхания и выведения больных из обморочного состояния, хлорид аммония NH4Cl как диуретик, оксид азота (I) N2O (веселящий газ) при простых операциях, в стоматологической практике и т. д.
Многие оксиды азота в высоких концентрациях являются высокотоксичными соединениями.
Фосфор и его соединения
Ортофосфорную кислоту применяют как реагент в неорганическом и органическом синтезе, полупродукт для получения минеральных удобрений, как компонент антикоррозийных покрытий, в пищевой промышленности и т. д.
Особое значение имеют фосфорсодержащие минеральные удобрения. Фосфор является необходимым элементом для жизнедеятельности растений, улучшения качества почв.
Соли фосфорной кислоты входят в состав азотно-фосфорных и азотно-фосфорно-калийных удобрений. Из них отметим аммофос, представляющий смесь моно- и диафосфатов аммония NH4H2PO4 и (NH4)2HPO4, а также нитрофоску — смесь NH4H2PO4, (NH4)2HPO4, CaHPO4, NH4NO3, KNO3, KCl.
Фосфор относится к органогенам. Его соединения составляют основу скелета и зубов животных и человека. Фосфор входит в состав белков и нуклеиновых кислот. Сахара и жирные кислоты могут быть использованы клетками в качестве источника энергии только при предварительном фосфорилировании.
Огромный интерес представляют фосфорорганические соединения. Среди них найдены эффективные лекарственные препараты, химические средства защиты растений. Наиболее токсичные и эффективные боевые отравляющие вещества (зарин, зоман, VX) также являются фосфорорганическими соединениями. Химия фосфорорганических соединений представляет собой огромный самостоятельный раздел элементоорганической химии.
Из неорганических соединений фосфора в медицинской практике применяют фосфаты алюминия AlPO4 и цинка Zn3(PO4)2, которые входят в состав фосфат-цементов, применяемых в стоматологии в качестве пломбировочного материала.
Кислород и его соединения
Кислород является органогеном. Он входит в состав всех жизненно важных органических веществ: белков, жиров и углеводов.
Без кислорода невозможны многочисленные жизненно важные процессы: дыхание, окисление аминокислот, жиров, углеводов.
В медицинской практике кислород применяют для вдыхания при болезненных состояниях, сопровождающихся кислородной недостаточностью, например заболевания дыхательных путей, сердечно-сосудистой системы и др.
Озон используют для дезинфекции помещений, обеззараживания воздуха и очистки питьевой воды. Небольшие примеси озона в воздухе улучшают состояние человека, особенно легочных больных.
Сера и её соединения
Сульфат кальция CaSO4 существует в виде двух кристаллогидратов: гипса CaSO4 × 2H2O и алебастра 2CaSO4 × H2O, применяют в строительстве и медицине для изготовления шин, повязок и т. д.
Сульфаты меди и железа используют для борьбы с вредителями растений.
Сульфат цинка ZnSO4 × 7H2O используют в качестве протравы для крашения тканей.
Сера относится к органогенам. Она входит в состав белков, аминокислот, гормонов, витаминов.
В медицинской практике применяют осаждённую серу как противоглистное средство. Осаждённая сера входит в состав ряда мазей и присыпок при лечении кожных заболеваний. Сульфат натрия Na2SO4 × 10H2O (глауберова соль) используется в качестве слабительного. Реже в медицинской практике применяют и другие соединения серы.
Фтор и его соединения
Соли фтористоводородной кислоты — неорганические фториды широко применяются в различных областях техники, например для разделения изотопов урана, синтеза хладагентов и т. д.
Жидкий фтор и некоторые из его соединений применяют в качестве окислителей ракетного топлива.
Соединения фтора обладают разнообразной биологической активностью. Фтор относят к микроэлементам. Его недостаток приводит к заболеванию, называемому гипофторозом, и проявляется кариесом зубов. При избыточном поступлении фтора в организм возникают различные формы флюороза и ряд профессиональных заболеваний. Практически все неорганические фториды являются высокотоксичными соединениями.
В медицинской практике используют фторид натрия NaF в виде полосканий, а также как добавку к зубной пасте.
Хлор и его соединения
Важное значение имеют следующие соединения хлора:
- Хлорид натрия NaCl применяют для получения гидроксида натрия, соляной кислоты, хлора, карбоната натрия, в мыловаренной и пищевой промышленности.
- Хлорид калия KCl применяют как калийное удобрение, для получения гидроксида и солей калия.
- Хлорид магния MgCl2 применяют для получения магния, цементов, в виде водных растворов — как средство против обледенения.
- Хлорид кальция CaCl2 применяют для получения кальция, как осушающий агент, его водные растворы используют в качестве хладагентов, средства против обледенения.
- Хлорид серебра AgCl применяют в фотографии.
- Хлорид алюминия AlCl3 применяют как катализатор в органическом синтезе.
- Хлорид железа (III) FeCl3 применяют как коагулянт при очистке воды, протраву при крашении.
- Хлорид ртути (I) Hg2Cl2 применяют как катализатор органических реакций, антисептик.
- Хлорид ртути (II) Hg2Cl применяют как протраву для семян, как катализатор в органическом синтезе.
- Хлорат калия KClO3 применяют в производстве взрывчатых веществ, спичек, для получения кислорода в лабораторных условиях.
- Хлорат кальция Ca(ClO3)2 применяют как окислитель в пиротехнике, гербицид, дефолиант для хлопчатника.
Хлор и его соединения обладают высокой биологической активностью и играют в организме человека важную роль. Хлор относится к сильнодействующим ядовитым веществам. Во время Первой мировой войны его использовали как боевое отравляющее вещество.
Хлорид-ион активирует некоторые ферменты, участвует в поддержании осмотического давления. В медицинской практике при недостаточной кислотности желудочного сока применяют разведенную соляную кислоту.
Раствор хлорида натрия 0,9% (изотонический) применяют при кровопотерях, интоксикациях, для растворения различных лекарственных веществ.
Гипертонические растворы хлорида натрия (3, 5, 10% соответственно) применяют в виде компрессов при лечении гнойных ран.
Хлорид кальция CaCl2 × 6H2O широко применяют как кровоостанавливающее средство, при аллергических заболеваниях и т. д.
Бром и его соединения
Применяют бром как бромирующий агент в органическом синтезе, для изготовления красителей и т. д.
Биологическая роль соединений брома выяснена недостаточно. В прошлом препараты брома NaBr и KBr широко применялись в качестве успокаивающих и противосудорожных средств. В настоящее время ими пользуются реже, но своего значения они не потеряли.
Йод и его соединения
Йод широко применяют в аналитической химии, в промышленности — для рафинирования тугоплавких металлов, как реагент в синтезе лекарственных препаратов.
Йод относится к числу незаменимых биогенных элементов. В организме он находится в связанном состоянии — в виде некоторых гормонов. Пары йода ядовиты. Как избыток, так и недостаток йода в организме приводит к различным заболеваниям.
В медицинской практике используют спиртовой раствор йода как антисептическое средство, а также йодид калия KI.
Железо и его соединения
Важнейшей областью применения железа является получение чугуна, стали и специальных сплавов.
Из солей железа в промышленности применяют железный купорос FeSO4 × 7H2O для приготовления минеральных красок, борьбы с вредителями растений; хлорид железа (III) FeCl3 как протраву при крашении ткани, коагулянт при очистке воды; сульфат железа (III) Fe2(SO4)3 × 9H2O как коагулянт и для травления металлов.
Железо является важнейшим биогенным элементом. Его общее содержание в организме человека составляет около 5 г. Большая часть железа содержится в гемоглобине крови, который обратимо связывает кислород и переносит его от легких к тканям. Кроме того, железо входит в состав ряда ферментов. Как избыток, так и недостаток железа в организме приводит к различным заболеваниям. Одним из самых серьёзных заболеваний, вызванных недостатком железа в организме, является гипохромная анемия. В медицинской практике используют более десяти различных препаратов железа, основу которых составляют FeCl3 × 4H2O, FeSO4 × 7H2O, лактат железа (II) [H3C–CH(OH)–COO]2Fe × 3H2O.
Тренировочные задания
1. Верны ли следующие суждения о правилах безопасного обращения с веществами в быту?
А. При работе с жидкими чистящими препаратами для ванн и раковин рекомендуется использовать резиновые перчатки.
Б. Растительное масло следует хранить вместе с препаратами бытовой химии.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
2. Верны ли следующие суждения о способах хранения веществ?
А. Кисломолочные продукты в открытой упаковке можно хранить длительное время.
Б. Витамин С выдерживает длительное кипячение в воде.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
3. Верны ли следующие суждения о приготовлении растворов и правилах безопасного обращения с веществами?
А. Готовить растворы кислот (уксусной, лимонной и др.) в домашних условиях в алюминиевой посуде не рекомендуется.
Б. При попадании раствора аккумуляторной серной кислоты на кожу рук следует промыть обожжённый участок водой и обработать раствором борной кислоты.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
4. Верны ли суждения о правилах применения и опасности для здоровья препаратов бытовой химии?
А. Стиральные порошки можно использовать для мытья посуды.
Б. Пары хлора полезны для здоровья.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
5. Верны ли суждения о правилах применения и хранения препаратов бытовой химии?
А. Аэрозоли, использующиеся в качестве средств для борьбы с бытовыми насекомыми, безопасны для детей и животных.
Б. Органические растворители являются негорючими жидкостями.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
6. Верны ли следующие суждения о видах смесей и препаратах бытовой химии?
А. Смесь растительного масла и воды является гомогенной смесью.
Б. Железо является жизненно важным элементом.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
7. Верны ли следующие суждения о способах приготовления растворов в химической лаборатории и о значении химических процессов в быту?
А. Для приготовления растворов кислот в химической лаборатории не следует брать алюминиевую посуду.
Б. Углекислый газ поддерживает горение.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
8. Верны ли следующие суждения о правилах безопасной работы в химической лаборатории и c препаратами бытовой химии?
А. В лаборатории наличие кислоты в растворе определяют на вкус.
Б. Оксиды серы и азота являются загрязнителями атмосферного воздуха.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
9. Верны ли следующие суждения о правилах безопасной работы в химической лаборатории и хранения веществ в быту?
А. При попадании раствора кислоты на кожу её следует промыть водой и обработать раствором питьевой соды.
Б. В состав всех органических веществ входит углерод.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
10. Верны ли следующие суждения о способах хранения веществ?
А. Промышленные консервы содержат в своём составе консерванты.
Б. Минеральные удобрения можно употреблять в пищу.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
11. Верны ли следующие суждения о способах приготовления растворов в химической лаборатории и быту?
А. Для приготовления раствора кислоты следует к концентрированной кислоте приливать воду.
Б. Раствор медного купороса, используемый для опрыскивания садовых деревьев, не следует хранить в оцинкованном ведре.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
12. Верны ли суждения о правилах применения и опасности для здоровья препаратов бытовой химии?
А. Стиральные порошки нельзя использовать для мытья посуды.
Б. Перекись водорода не повреждает волосы при контакте.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
13. Верны ли суждения о правилах применения и хранения препаратов бытовой химии?
А. Аэрозоли, использующиеся в качестве средств для борьбы с бытовыми насекомыми, безопасны для детей и животных.
Б. Органические растворители являются горючими жидкостями.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
14. Верны ли следующие суждения о влиянии химических веществ на окружающую природную среду и составе средств гигиены?
А. Промышленные выбросы оксидов азота и серы вызывают кислотные дожди.
Б. Зубная паста, содержащая ионы железа, способствует укреплению зубной эмали.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
15. Верны ли следующие суждения о биологической роли химического элемента и об использовании химических реакций для оказания человеку первой помощи?
А. Без кислорода жизнь человека невозможна.
Б. Раствор питьевой соды используется для обработки участка кожи, на который попала кислота.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
16. Верны ли следующие суждения о смесях и составе моющих средств?
А. Раствор аммиака в воде (нашатырный спирт) — это гомогенная смесь.
Б. В состав мыла входит стеарат натрия.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
17. Верны ли следующие суждения о химическом элементе и значении средств гигиены?
А. Алюминий является основным металлом в авиастроении.
Б. Зубная паста, содержащая ионы фтора, способствует укреплению зубной эмали.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
18. Верны ли следующие суждения о химическом элементе и препаратах бытовой химии?
А. Соединения кальция являются основой бетона.
Б. Отбеливающие препараты бытовой химии безопасны для человека и животных.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
19. Верны ли суждения о химическом загрязнении окружающей среды и его последствиях?
А. Повышенное содержание в замкнутом пространстве оксида углерода (II) не является угрожающим фактором для здоровья человека.
Б. Производство чугуна и стали является источником загрязнения атмосферы.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
20. Верны ли суждения о химическом загрязнении окружающей среды и его последствиях?
А. Повышенное содержание в атмосфере оксидов азота оказывает благотворное влияние на здоровье человека.
Б. Наличие неорганических щелочей в промышленных стоках положительно влияет на жизнедеятельность рыб в водоёмах.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны