Урок 23. Понятие о кислотах
В уроке 23 «Понятие о кислотах» из курса «Химия для чайников» познакомимся со сложными веществами — кислотами; узнаем об индикаторах и как они помогают человеку.
В тексте нашего учебника вам уже неоднократно встречалось слово «кислота». Много раз, конечно, вы слышали это слово и в повседневной жизни. При приготовлении пищи используются уксусная и лимонная кислоты, в домашней аптечке есть борная кислота, в аккумуляторы автомашин заливают серную кислоту и т. д. Отметим, что и в быту, и в производственной деятельности людей используются в основном водные растворы кислот. Познакомимся поближе с этими веществами.
Состав кислот
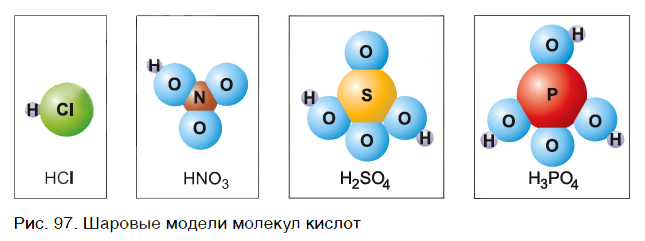
В большинстве случаев в состав молекул кислот входят только атомы неметаллов. На рисунке 97 представлены шаровые модели молекул некоторых кислот и их формулы. Что общего у этих молекул? Ответ прост — в них входят атомы водорода.
Обратим внимание, что в состав молекулы хлороводорода, кроме атома водорода Н, входит атом хлора Cl, молекулы азотной кислоты — группа атомов NO3, молекулы серной кислоты — SO4, молекулы фосфорной кислоты — PO4.
Атом Cl, группы атомов NO3, SO4, PO4, а также другие атомы и группы атомов в составе кислот называют кислотными остатками.
Кислоты — сложные вещества, в состав которых входят атомы водорода, способные замещаться атомами металлов, и кислотные остатки.
Кислотные остатки в молекулах кислот соединены с атомами водорода в соответствии со своей валентностью. Как можно ее определить? Водород всегда одновалентен. Значит, если кислотный остаток в молекуле кислоты соединен с одним атомом водорода, то его валентность равна единице, если с двумя атомами — двум, а с тремя — трем.
При написании формул кислот сначала пишут атомы водорода, а потом кислотные остатки.
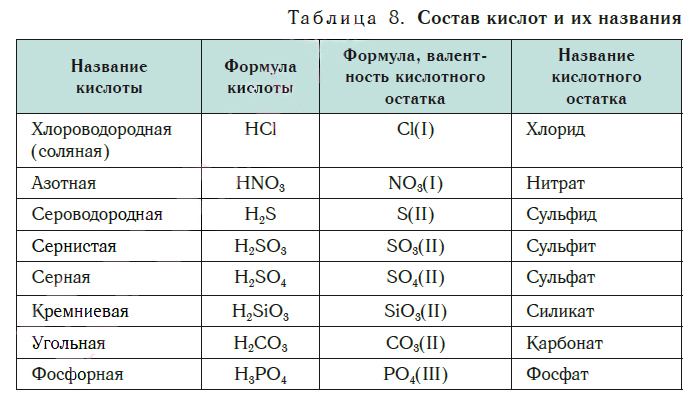
В таблице 8 представлены названия и формулы кислот, с которыми вы будете встречаться при изучении основ химии. Здесь же даны формулы кислотных остатков, которые входят в состав этих кислот, их валентность и названия.
При обычных условиях кислоты существуют в жидком и твердом агрегатных состояниях. Так, фосфорная кислота H3PO4 при комнатной температуре — твердое вещество. При этих же условиях серная кислота H2SO4 — это не имеющая запаха вязкая жидкость. Она почти в 2 раза тяжелее воды. Хлороводородная кислота HCl — раствор газа хлороводорода в воде. Она имеет еще и историческое название «соляная кислота». Раствор этой кислоты имеет характерный запах.
В большинстве случаев кислоты растворяются в воде. Исключение — кремниевая кислота H2SiO3. Водные растворы хлороводородной, серной и фосфорной кислот не имеют окраски. Безводная азотная кислота при хранении желтеет.
Поскольку в состав всех кислот входят атомы водорода, то кислоты обладают общими свойствами: 1) изменяют окраску некоторых органических веществ; 2) имеют кислый вкус (пробовать кислоты на вкус, как и любые другие вещества, запрещается — можно получить ожог полости рта!); 3) оказывают разъедающее действие на кожу человека, ткани, бумагу, древесину и другие материалы.
Есть вещества, которые, как и кислоты, содержат атомы водорода, но кислотными свойствами не обладают, например метан CH4, аммиак NH3, вода H2O и др. Следовательно, не все вещества, содержащие атомы водорода, относят к кислотам.
Меры предосторожности при работе с кислотами
Кислоты — едкие вещества. Попадание кислот на кожу или в глаза может привести к болезненным химическим ожогам. Обращаться с кислотами нужно очень осторожно. При работе с ними следует надевать специальные халаты, перчатки, очки. При попадании кислоты на кожу или в глаза ее необ ходимо немедленно смыть большим количеством воды, а затем пораженный участок промыть раствором питьевой соды. В случае необходимости следует обратиться в медпункт.
Понятие об индикаторах
Некоторые органические вещества изменяют свою окраску в присутствии кислот и ряда других веществ. Такие вещества называют индикаторами, что в переводе с латинского означает «указатель».
Индикаторы — это органические вещества, которые изменяют свою окраску в присутствии кислот и ряда других веществ.
На уроках химии для обнаружения в растворах кислот используют индикаторы лакмус, метиловый оранжевый (метилоранж), а также универсальный индикатор. Это полоска фильтровальной бумаги, пропитанная смесью индикаторов. Окраска индикаторов в воде показана на рисунке 98. Индикаторы изменяют свой цвет, если в растворе есть кислоты (рис. 99).
На заметку: В растворах кислот изменяют цвет сок краснокочанной капусты, вишни, черноплодной рябины, цветки фиалки и др.
Краткие выводы урока:
- В состав кислот входят атомы водорода и кислотные остатки.
- Индикаторы — органические вещества, изменяющие свою окраску в присутствии кислот и ряда других веществ.
Надеюсь урок 23 «Понятие о кислотах» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.